強塩基といえば、NaOHを思い浮かべる人が多いだろう。確かに、水中では水酸化物イオン(OH–)が最強と考えても差し支えないだろう。しかし、話を気相中に広げれば、まだまだ上があるのだ。
とはいえ、そもそも塩基の強さってどうやって比較したら良いのだろうか?よく使われるのがプロトン親和力を用いる方法だ。例えば、水酸化物イオン(OH–)のプロトン親和力は水中で1633 kJ/molである。
気相中で最強の塩基はというと、ごく最近までLithium monooxide anion(LiO–)であるとされ、そのプロトン親和力は1782 kJ/molと報告されている[DOI: 10.1073/pnas.0801393105]。
ところが、これよりも更に強い塩基が新たに報告された(2016年の情報)。それは、o-diethynylbenzene dianion(下図)で、そのプロトン親和力はなんと1843 kJ/mol [DOI: 10.1039/C6SC01726F]。これは、気相中でベンゼンからプロトンを引き抜いちゃうくらい強力な塩基だ。
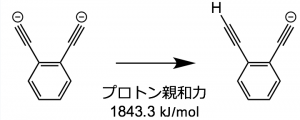
そんな強い塩基をどうやって発生させるかという工夫もなかなか興味深い。対応するジカルボン酸をESIマスで陰イオン化することで、段階的な脱炭酸反応を経たジアニオン生成反応を使ってはじめてこうした化学種を発生させることができる。こういうナイスアイデアが、研究をググっと前進させるから化学って面白い。
で、多くの人が、この記録は抜けないだろうって考えているようですが、単純に、エチニルを6本生やしたhexaethynylbenzene hexa-anion(下図)はいかがでしょうか?
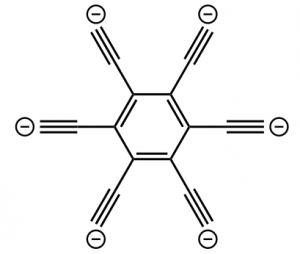
も〜、脱炭酸に次ぐ脱炭酸で、エイヤと作る。ポイントは、ESIマスの装置の性能だから、これは分子研の出番かとも思う。きっと誰かがやってくれると期待しています。
もう一点、このエチニル基の置換位置によるプロトン親和力の違いが興味深い。オルト位の親和力が一番高く、メタ位がその次(1787 kJ/mol)、そしてパラ位が一番低い(1781 kJ/mol)となっていて、オルト位の効果が出ているのだ。これは、Hammet屋が黙っていないのではないだろうか?そのあたりの研究についても、今後を期待したい!
もし、自分がこの系で研究するなら、光をトリガーとしたヘキサエチニルベンゼンヘキサアニオン(上図)の発生かとも思う。ケージド化合物のアプローチで、不安定化学種をエイヤと作るのは、いろいろと夢のある話だ。
だから化学は止められない。